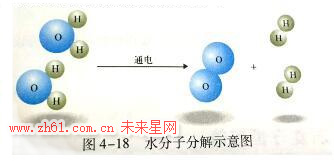
如图所示:
水是由氢和氧两种元素按2:1的比例组成的无色无嗅无味透明的无机液体,它广泛分布在地球表面;它是生命的重要组成部分,地球上正是有了大量液态水才孕育出生命,我们可以一天不吃东西,但没有办法一天不呼吸,也必须每天补充水。
水分子具有弯曲型结构,O ―H 键长 95. 72pm , HOH 键角 104. 52°,O ―H 键和孤对电子形成四面体构型的分布,2 个键对电子与 2 个孤对电子按四面体型分布在 4 个顶点上。
水是极性分子,分子偶极矩μ= 6. 17 *10 - 30 Cm 。水分子的这种四面体构型以及能够从4 个方向和其他分子形成氢键的能力,是了解一切含水化合物中水的结构和性能的基础。
扩展资料
水的物理特性与水分子间的氢键有很大关系:
一个大气压下,当水的温度在0℃~3.98℃时,水中大多是两个bO或三个bO分子抱成团,形成(bO)2和(bO)3缔合分子,这时候水分子间的距离最近,水的密度最大;
温度升高,缔合分子越来越少,水开始膨胀;当温度上升到100℃,水分子间的氢键断开,单个的水分子变成水蒸气;
而温度降低到0℃以下时,水开始结冰,所有的bO分子会聚合成一个巨大的分子团,由于水分子力场的关系,氧原子会与附近两个水分子的氢原子结成氢键,这种晶体结构造成更大的空隙,使体积膨胀。这就是冰的密度比水低、会浮在水面的原因。
参考资料来源:百度百科-水
2.N2 CO2 bO NH3 CH4 C2b的结构式我按上面顺序答啦 空间结构 直线型 直线型 折线型 三角锥型 四面体型 直线型 结构式 (氮氮三键) (两个碳氧双键排成直线) (两个氢氧键成104.5度大概) (三个氮氢单键成一定角度即可,一般把氮写在上面) (画个正四面体,碳在中心,氢在端点,单键相连) (碳碳三键,两边接氢) 电子式按结构式类推即可,记得氮要画孤电子对(补齐原子周围八电子即可,除氢外) 键的极性: 相同元素原子成键为非极性,其余为极性,根据结构式类推 分子的极性: 非极性 非极性 极性 极性 非极性 非极性。

 更多
更多
 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底