如果两个热力学系统中的每一个都与第三个热力学系统处于热平衡(温度相同),则它们彼此也必定处于热平衡。这一结论称做"热力学第零定律"。(zeroth law of thermodynamics:The zeroth law states that if two systems are in thermal equilibrium with a third system, they are also in thermal equilibrium with each other.)
基本信息
中文名称:热力学第零定律
外文名称:zeroth law of thermodynamics
提出者:拉尔夫・福勒(R.H.Fowler)
应用学科:物理,化学等
适用领域范围:物理,化学领域
最常见的应用:制造温度计
内容
热力学第零定律的重要性在于它给出了温度的定义和温度的测量方法。定律中所说的热力学系统是指由大量分子、原子组成的物体或物体系。它为建立温度概念提供了实验基础。这个定律反映出:处在同一热平衡状态的所有的热力学系统都具有一个共同的宏观特征,这一特征是由这些互为热平衡系统的状态所决定的一个数值相等的状态函数,这个状态函数被定义为温度。而温度相等是热平衡之必要的条件。
通常表述
热力学中以热平衡概念为基础对温度作出定义的定律。通常表述为:与第三个系统处于热平衡状态的两个系统之间,必定处于热平衡状态。图中A热力学第零定律示意图、B热力学第零定律示意图、C热力学第零定律示意图为3个质量和组成固定,且与外界完全隔绝的热力系统。将其中的B、C用绝热壁隔开,同时使它们分别与A发生热接触。待A与B和A与C都达到热平衡时,再使B与C发生热接触。这时B和C的热力状态不再变化,这表明它们之间在热性质方面也已达到平衡。第零定律表明,一切互为热平衡的系统具有一个数值上相等的共同的宏观性质──温度。温度计所以能够测定物体温度正是依据这个原理。
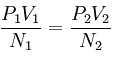
另一种表述
处于热力学平衡状态的所有物质均具有某一共同的宏观物理性质。
适用范围
第零定律是在不考虑引力场作用的情况下得出的,物质(特别是气体物质)在引力场中会自发产生一定的温度梯度。如果有封闭两个容器分别装有氢气和氧气,由于它们的分子量不同,它们在引力场中的温度梯度也不相同。如果最低处它们之间可交换热量,温度达到相同,但由于两种气体温度梯度不同,则在高处温度就不相同,也即不平衡。因此第零定律不适用引力场存在的情形。这与限定第二类永动机不成立的第二定律类似。
温度关系
第零定律经常被认为可以建立一个温度函数;更随便的说法是可以制造温度计。而这个问题是其中一个热力学和统计力学哲学的题目。
在热力学变量的函数空间之中,恒温的部分会成为一块面并会为附近的面提供自然秩序。之后,该面会简单建立一个可以提供连续状态顺序的总体温度函数。该恒温面的维度是热力学变量的总数减一(例如对于有三个热力学变量 P、V、n 的理想气体,其恒温面是块二维面)。按此定义的温度实际上未必如摄氏温度尺般,而是一个函数。
以理想气体为例,若两团气体是处于热平衡,则:
Pi 是第 i 个系统的压强Vi 是第 i 个系统的体积Ni 是第 i 个系统的数量(摩尔数或者原子数目)面 PV / N = const 定义了所有相同温度的面,一个常见方法来标签这些面是令 PV / N = RT,R 是一个常数而温度 T 可以由此定义。经定义后,这些系统可用作温度计来较准其他系统。
意义
热力学第零定律用来作为进行体系测量的基本依据,其重要性在于它说明了温度的定义和温度的测量方法。表述如下:
1.可以通过使两个体系相接触,并观察这两个体系的性质是否发生变化而判断这两个体系是否已经达到热平衡。
2.当外界条件不发生变化时,已经达成热平衡状态的体系,其内部的温度是均匀分布的,并具有确定不变的温度值。
3.一切互为平衡的体系具有相同的温度,所以一个体系的温度可以通过另一个与之平衡的体系的温度来表示,也可以通过第三个体系的温度来表示。
ps:初中物理公式,热学部分:1,吸热:Q吸=Cm(t-t0)=Cmt;2,放热:Q放=Cm(t0-t)CMt;3,热力学温度:T=t+273k。在大学物理中Cm与温度t有关。

 更多
更多
 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底