原子结构示意图的书写规则(方法一)
规则一:从内往外数
第一层(K层)最多不超过2个电子;
第二层(L层)最多不超过8个电子;
第三层(M层)最多不超过18个电子;
第四层最多(N层)不超过32个电子。
规则一需要补充三点:
第一,每层电子的最多数目符合2n2(n代表电子层序数);
第二,也就是数到第四层,第五层电子数目前不符合2n2;
第三,“最多”代表可以少于这个数,可以等于这个数。
规则二:从外往内数
倒数第一层最多不超过8个电子;
倒数第二层最多不超过18个电子;
倒数第三层最多不超过32个电子。
规则二也需要补充两点:
第一,只能数到倒数第三层,因为目前的原子结构示意图,最多就七层。正着数和倒着数记起来正好是七层。
第二,“最多”代表可以少于这个数,也可以等于这个数。
规则三:周期数=电子层数;最外层电子数=主族序数。
因此,只要确定了一个元素在周期表中所在的位置,基本上不用经过大脑,就可以秒写出它的原子结构示意图。不信吗?我们举个例子。
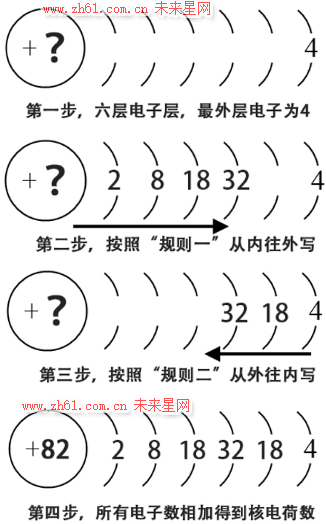
例如铅(Pb),我们通过查阅元素周期表,知道它是第六周期、第IVA族的元素,利用规则三可知,其最外层电子数为4,一共有6层电子层。
最终通过三个规则和四步操作,确定了Pb的原子结构示意图和原子序数。
那么问题来了,我们有没有办法不查阅元素周期表,就直接知道Pb是第六周期、第IVA族吗?答案是肯定的,但是需要你付出一点脑细胞。只要你竖着背下来元素周期表(仅限主族和0族),那么你就会很快推算出来Pb在元素周期表中的位置,以及它的原子序数/核电荷数/质子数(所有的电子数目加起来即原子序数)。
一、氢锂钠钾铷铯钫
二、铍镁钙锶钡镭
三、硼铝镓铟铊
四、碳硅锗锡铅
五、氮磷砷锑铋
六、氧硫硒碲钋
七、氟氯溴碘砹
八、氦氖氩氪氙氡
以上这些像咒语一样的玩意儿,你必须反复念,念到滚瓜烂熟为止,念到一提起铅,马上脱口而出:碳硅锗锡铅。同时,我们对碳族中的碳非常熟悉,知道它是第二周期的元素,那么跟着一起念,碳硅锗锡铅,二三四五六。从而确定铅是第六周期的元素。又知整个碳族元素都是第IVA族,最后确定Pb为第六周期、第IVA族的元素。
原子结构示意图的书写规则(方法二)
首先,我要说明的是方法二也是建立在方法一的基础上,但采用的是0族参考系法。这是什么意思呢?且听我慢慢道来。
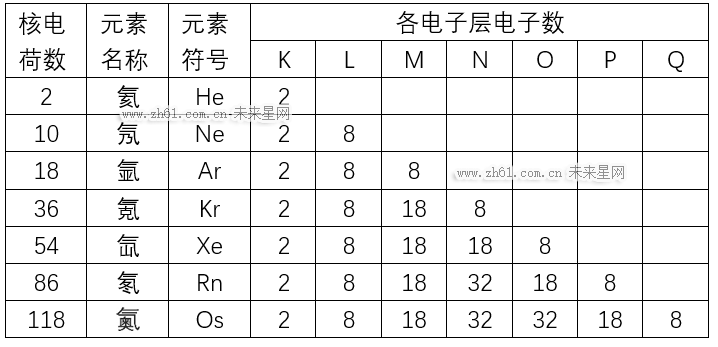
在教材87页的“思考与讨论”中,给出了0族元素的原子结构示意图(我们可以加上118号元素Og,下方表格里的元素符号有误)。
写成常规的格式,即:
我们记住了所有0族元素的原子结构示意图,以它们为参考系,就可以快速写出左邻右舍元素的原子结构示意图了。例如,54号元素Xe的原子结构示意图为:
可以推知,前面的52号元素的原子结构示意图为:
从而可以断定它是52号元素,处在第五周期、第VIA族。
再加上竖着背下来元素周期表的能力加持,第VIA族,氧硫硒碲钋,二三四五六,即碲(Te)元素。
再例如,54号元素Xe后面就是第六周期的第一个元素――第IA族的碱金属55号元素。
其原子结构示意图为:
s区元素的原子结构示意图略有不同
在元素周期表中,第IA族、第IIA族的元素统称为s区元素,它们的原子结构示意图与第IIIA族~第0族(统称为元素周期表的p区元素)的写法有点不一样。
我们还是以55号元素铯(Cs)为例来说明,总结一下s区元素的原子结构示意图的写法:
规则一:从内往外数,每层的电子数依然符合2n2。
规则二:从外往内数,最外层电子数为1或2,次外层电子数为8(三层及其以上符合),倒数第三层的电子数为18个(五层及其以上符合),倒数第四层的电子数为32个(仅限钫Fr)。
规则三:周期数=电子层数,最外层电子数=主族序数。

 更多
更多

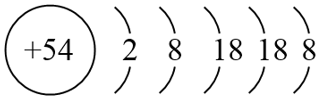
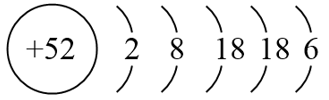
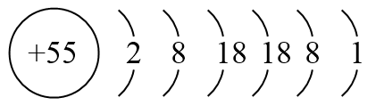

 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底