
2020年高考全国一卷理综化学35题:[化学一选修3:物质结构与性质]Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题: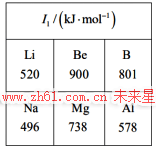
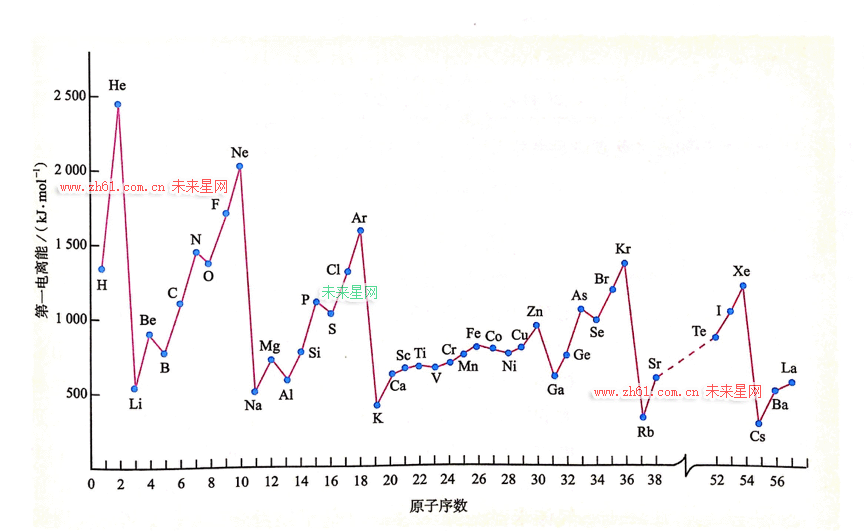
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)> I1(Na),原因是_________。I1(Be)> I1(B)> I1(Li),原因是________。
【答案】(2). Na与Li同主族,Na的电子层数更多,原子半径更大,故第一电离能更小 (3). Li,Be和B为同周期元素,同周期元素从左至右,第一电离能呈现增大的趋势;但由于基态Be原子的s能级轨道处于全充满状态,能量更低更稳定,故其第一电离能大于B的。 Be的第一电离能为什么高于B?有的课堂对此的解释是:Be的价电子为2s2,全满稳定。需要指出的是,这是不准确的解释。本文进行详细阐述。
在同一能级的简并轨道中自旋方向相同的电子,彼此间是不可区分而且可以互相交换的,比如C的2px1电子与2py1电子在“运动”过程中可以互相交换,并且交换后无法区分彼此(区分这两个电子也是没有意义的一件工作)。在电子交换的过程中会放出能量,使原子体系获得一个额外的稳定性。自旋平行的一对电子失去一个时,交换能也随之消失。因此,电子在同一能级的简并轨道上以自旋平行方式排列比自旋相反排列的方式更稳定(因为自旋相反的两个电子不能交换,也就不会放出交换能使原子体系更稳定)。
显然地,p能级或d能级的最高的交换能出现在他们的半满结构,所谓半满结构是同一能级的所有轨道各自填充一个自旋平行的电子。能级达到半满结构时,以自旋平行方式存在的电子数目最大。导致的结果是半满结构是一种非常稳定的排布方式,如N原子的2p能级电子组态为2px12py12pz1,从这种排布移除一个电子时需要额外输入能量以克服这一最大的交换能(由于自旋相同的电子交换时释放能量,所以去掉一个平行自旋的电子时,体系就要吸收相应的能量)。Cr原子的电子组态为3d54s1而非3d44s2,就是因为前者的3d轨道达到半满结构,轨道具有最大的交换能(别忘记交换能指放出能量),从而使体系更稳定。p能级和d能级的全满结构也存在最大交换能(两组自旋方向相同的电子都达到最大数量),因此全满也有额外的稳定性。
显然地,s能级只有一个轨道,无论其半满还是全满,都不存在交换能,s能级的半满或全满结构都不会给原子体系带来额外的稳定性,因此谈论s能级的半满或全满态,对于稳定性的讨论是没有作用的。
新人教版物构教材
新苏教版物构教材
一.洪特规则的定义
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,而且自旋状态相同。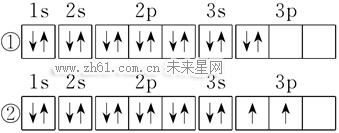
根据洪特规则的定义,①不符合洪特规则,①中3P能级里的2个电子应该优先单独占据一个轨道,而且自旋状态相同。②符合洪特规则的规定。
二、适用范围
洪特规则只适用于LS 耦合的情况。有少数例外是由于组态相互作用或偏离LS耦合引起的。该定则可用量子力学理论和泡利不相容原理来解释。该定则对确定自由原子或离子的基态十分有用。
三、洪特规则的解释
洪特规则之一
洪特规则是在等价轨道(指相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同。后来经量子力学证明,电子这样排布可能使能量最低,所以洪特规则也可以包括在能量最低原理中。洪特规则之二(洪特规则的补充规定)
洪特规则又称等价轨道规则。在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同。如氮原子中的3个p电子分布于3个p轨道上并取向相同的自旋方向。洪特规则指出,等价轨道上的电子排布处于以下状态时比较稳定。
(1)全充满:p6、d10、f14p轨道上有6个电子、d轨道上有10个电子、f轨道上有14个电子
(2)半充满:p3、d5、f7p轨道上有3个电子、d轨道上有5个电子、f轨道上有7个电子
(3)全空:p0、d0、f0p轨道上有0个电子、d轨道上有0个电子、f轨道上有0个电子
洪特规则特例
举例:(以铬为例)按照能量最低原理,铬的电子排布式为1s22s22p63s23p63d44s2但根据洪特规则的补充规定,铬的电子排布式实际为1s22s22p63s23p63d54s1,这种排布符合半充满状态,可使能量最低。(以铜为例)按照能量最低原理,铜的电子排布式为1s22s22p63s23p63d94s2但根据洪特规则的补充规定,铬的电子排布式实际为1s22s22p63s23p63d104s1,这种排布符合全充满、半充满状态,可使能量最低。
像铁离子Fe3+(3d5)和亚铁离子Fe2+(3d6)对比看,从3d6→3d5才稳定,这和亚铁离子不稳定易被氧化的事实相符合。根据洪特规则铬的电子排布式应为1s22s22p63s23p63d54s1。 s轨道有全满和半满吗?
p3 d5 f7 为半充满,那s1可以算半充满吗?
洪特规则的例外很多例如“原子轨道中,每一层半满或全满时能量最低”,也就是说s1、2,p3、6,d5、10,f7、14的时候能量最低也最稳定,是原子存在的一般形式。
s轨道全满和半满哪一个更稳定?钾(4s1)的第一电离能低于钙(4s2)的第一电离能,因为全满更稳定,所以钙比较难电离,而且钙离子中心电荷大,吸引力强,也可以解释其第一电离能较高。想想s轨道全满和半满的两个例子全满Mg半满Na在周期表上相邻,Mg的金属性远远弱于Na,可见半满的稳定性远远小于全满。 所有情况都符合吗? 只要看元素周期表就会发现,排在下面几行的几类元素,尤其是镧系和锕系元素没有几个符合洪特规则,这也是理论所无法解释的。 遇到的问题 根据洪特规则中关于全充满、半充满、全空的规定,学生在写碳的电子排布式时出现了这样的情况,碳的电子排布式本来应该是1s22s22p2,结果学生按照全充满、半充满、全空的规定,将碳的电子排布式写成了1s22s12p3。我表扬了这名学生,她严格的遵循定义,学以致用,说明她进行了一定的思考。但是这里也有些更高层次的原因,导致1s22s12p3的写法是错误的。
碳的电子排布式中不遵循全充满、半充满、全空的规定的原因是:碳的2s和2p轨道之间能量相差比较大,其中一个2S电子如果放到2P上能量反而比2s22p2的电子构型能量要高,前者是激发态。对于第四周期的元素,因为3d和4s轨道之间的能量差距不是很大,所以对于Cr和Cu,按洪特规则排布能量更低。 附:洪特规则还有一个量子力学叙述:洪特规则是原子物理学中对LS耦合电子组态的能级顺序的一个规则,于1925年由德国物理学家Friedrich Hund提出。洪特规则指出,对于一个给定的电子组态形成的一组原子态,总自旋量子数Ms最大的能量最低,总自旋量子数S相同时,总角量子数L最大的能量最低。1927年洪特又提出了附加规则:对于同一支壳层的同颗电子,如果电子数不足或等于满壳层电子数的一半,总角量子数l越小能级越低,称为正常次序;如果电子数超过满壳层电子数的一半,总角量子数J越大能级越低,称为倒转次序。例如,氦原子P能级的三重态即为倒转顺序。

 更多
更多


 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底